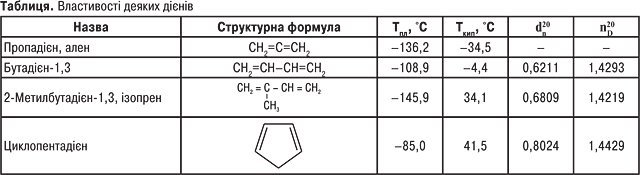
ДІЄНОВІ ВУГЛЕВОДНІ (дієни, діолефіни) — ненасичені вуглеводні, молекули яких містять два подвійних зв’язки. Розрізняють аліфатичні Д.в. СnН2n–2 — алкадієни (діолефіни) та аліциклічні СnН2n–4 — циклоалкадієни. За взаємним розміщенням подвійних зв’язків алкадієни поділяють на три групи: з кумульованими подвійними зв’язками (аленові вуглеводні), в яких подвійні зв’язки знаходяться біля одного атома карбону; з кон’югованими подвійними зв’язками (спряжені), в яких подвійні зв’язки розташовані на відстані одного σ-зв’язку; з ізольованими подвійними зв’язками, коли подвійні зв’язки знаходяться на відстані більшій, ніж один σ-зв’язок. Назви Д.в. за систематичною номенклатурою утворюють, додаючи до кореня відповідного насиченого вуглеводню суфікс -дієн, цифрою вказують розташування кожного з подвійних зв’язків у головному вуглеводневому ланцюгу; для деяких Д.в. збереглися тривіальні назви: СН2=С=СН2 — ален, пропадієн,  — ізопрен, 2-метилбутадієн-1,3 (таблиця). Алкадієни — безбарвні речовини. Перші члени гомологічного ряду — гази або низькокиплячі рідини.
— ізопрен, 2-метилбутадієн-1,3 (таблиця). Алкадієни — безбарвні речовини. Перші члени гомологічного ряду — гази або низькокиплячі рідини.
Особливості будови Д.в. різних типів знайшли відображення в їх реакційній здатності. Д.в. з ізольованими та кумульованими подвійними зв’язками за хімічними властивостями нагадують алкени (олефіни), тільки в реакцію вступає не один, а два зв’язки з більшою або меншою селективністю. Алени мають деякі особливості. Електрофільне та радикальне приєднання до аленів проходить легше, ніж до олефінів, за рахунок двох сусідніх подвійних зв’язків. Аленовий зв’язок під дією кислот та лугів може ізомеризуватися в ацетиленовий або 1,3-дієновий:

Система зв’язків в аленах лінійна: два π-зв’язки та кінцеві замісники розташовані у взаємноперпендикулярних площинах, тому несиметричні заміщені алени існують у вигляді енантіомерів. У Д.в. з кон’югованими подвійними зв’язками атоми спряженої системи знаходяться у стані sp2-гібридизації і розташовані в одній площині, при цьому відбувається часткова делокалізація π-електронної густини зі зменшенням енергії системи та вирівнюванням міжатомних відстаней, що приводить до підвищеної поляризованості молекул, аномально високих показників заломлення світла (екзальтації молекулярної рефракції). Єдина спряжена система у Д.в. зумовлює їх підвищену реакційну здатність порівняно з олефінами та особливості хімічної поведінки. Для кон’югованих Д.в. характерні реакції електрофільного приєднання як за одним подвійним зв’язком (1,2-приєднання), так і за кінцями системи спряжених зв’язків з переміщенням подвійного зв’язку (1,4-приєднання). Співвідношення продуктів залежить від умов проведення реакції та природи реагенту. Приєднання галогеноводнів, галогенів призводить до утворення суміші продуктів. При підвищенні температури та переході від хлору до йоду вихід продукту 1,4-приєднання зростає:

Водень у момент виділення зі спряженими Д.в. утворює продукт 1,4-приєднання, а за наявності каталізаторів (Ni, Pt) утворюється суміш продуктів. Аліфатичні спряжені Д.в. полімеризуються та співполімеризуються з різноманітними вініловими мономерами. Як ініціатори реакції найчастіше застосовують металоорганічні сполуки, лужні метали, неорганічні та органічні пероксиди. Утворення полімерів відбувається переважно за типом 1,4-приєднання:

Реакцію використовують у виробництві синтетичних каучуків, термопластів. Спряжені Д.в. приєднують речовини, які містять подвійні чи потрійні карбон-карбон зв’язки (дієнофіли) з утворенням циклічних структур:

Реакція відома під назвою «дієновий синтез» або реакція Дільса — Альдера і використовується для синтезу поліциклічних структур, ідентифікації і кількісного визначення Д.в. Промислове застосування знайшли методи одержання спряжених Д.в. шляхом каталітичного дегідрування алканів, алкенів за наявності Cr2O3 або Al2O3. Д.в. також виділяються у процесі крекінгу нафти (напр. бутан-бутенової фракції):

Їх можна отримати шляхом дегідратації ненасичених спиртів або діолів за наявності мінеральних кислот та оксиду алюмінію:

Термічне перетворення етанолу шляхом каталітичної дегідратації на змішаному каталізаторі (ZnO/Al2O3) застосовується для промислового одержання бутадієну-1,3 (метод С.В. Лебєдєва). Відомі способи одержання спряжених дієнів дегідрогалогенуванням насичених дигалогенідів, частковим гідруванням вінілацетиленів, розщепленням 1,4-діамінів та ін.
Алени поширені серед метаболітів морських гідробіонтів, комах, вищих рослин та грибів; їх використовують в органічному синтезі як проміжні продукти для синтезу лікарських речовин: простагландинів, вітамінів, феромонів. Кон’юговані Д.в. (циклопентадієн) у промисловості застосовують для синтезу ізадрину, антипіренів, інсектицидів (альдрин), синтетичних каучуків, смол, пластифікаторів, поліамідних волокон.
Губин С.П., Голоунин А.В. Диены и их π-комплексы. — Новосибирск, 1983; Марч Дж. Органическая химия. — Т. 3. — М., 1987; Черных В.П., Зименковский Б.С., Гриценко И.С. Органическая химия / Под общ. ред. В.П. Черных. — 2-е изд. — Х., 2007; Фельдблюм В.Ш. Синтез и применение непредельных циклических углеводородов. — М., 1982; The chemistry of ketenes, allenes, and related compounds / Еd. S. Patai. — 1980. Vоl. 1–2, № 4.
